Regulatorischer Lebenszyklus
Wir helfen Medizintechnikunternehmen überall auf der Welt, die neuen, umfassenden Anforderungen und Compliance-Erwartungen während des gesamten Produktlebenszyklus zu erfüllen.
.png)
Der regulatorische Lebenszyklus
Medizinprodukte sind weltweit reguliert. Da jedoch die Definitionen von Medizinprodukten in den verschiedenen Teilen der Welt variieren und auch die Klassifizierungen unterschiedlich sind, können die erforderlichen Zulassungsaktivitäten variieren. Es ist von Vorteil, in den Zulassungsplänen die Zielmärkte zu benennen, um die Aktivitäten besser planen zu können. Das ermöglicht reibungslose globale Registrierungen und kürzere Markteinführungszeiten. Wenn Sie also ein Produkt zuerst für die USA und danach für die EU und Australien planen, lohnt es sich, das Produkt für alle geplanten Zielmärkte zu qualifizieren und zu klassifizieren. Das gilt besonders, wenn das Produkt auf dem ursprünglichen Zielmarkt, z.B. den USA, nicht als Medizinprodukt gilt, aber in den anderen Ländern als Medizinprodukt eingestuft wird. Solche Situationen können erheblichen Einfluss auf die konkret erforderlichen Entwicklungsaktivitäten haben. Labquality hat Erfahrung mit zahlreichen Märkten.
Auslegung
Viele Aspekte einer technischen Dokumentation sind in den meisten Ländern identisch. Eine vereinfachte Ablaufdarstellung könnte so aussehen:
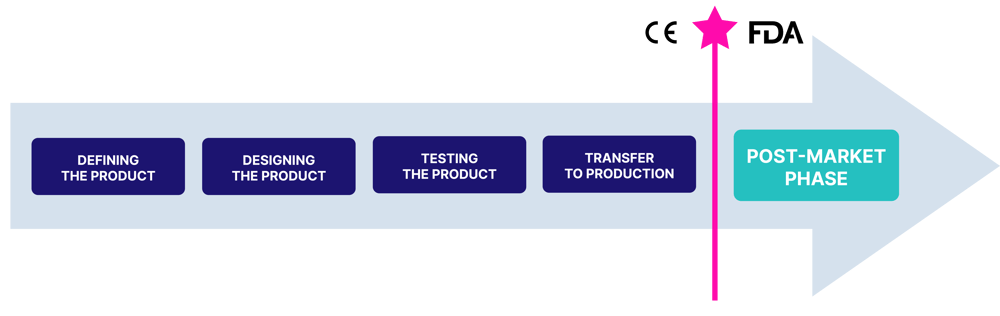
Der Auslegungsgesamtprozess muss vom Auslegungs- und Entwicklungsprozess (oder der Designlenkung) des Fertigungsunternehmens abgedeckt werden. Dabei werden in erster Linie die Anforderungen und Risiken ermittelt: Was wollen die Anwender*innen, welche Anforderungen gelten und welche Risiken sind damit verbunden? Das ist überall ähnlich. Allerdings müssen die Anforderungen und Risiken alle erforderlichen Aspekte berücksichtigen. Zu dem Team, das sich damit befasst, muss eine Person gehören, die mit Anforderungs- und Risikomanagementprozessen vertraut ist. Wir beschäftigen Fachkräfte, die Sie in dieser Hinsicht unterstützen können.
Nach der Definitionsphase wird das Produkt entworfen, getestet und in die Produktion überführt. Bei jedem dieser Schritte fällt ein beträchtliches Volumen an Nachweisunterlagen an: Spezifikationen, Testpläne und Testberichte, Arbeitsanweisungen und die technische Produktdokumentation. Ein wesentlicher Konformitätsnachweis ist der klinische Nachweis. Insbesondere die EU-Verordnungen haben die Anforderungen in diesem Bereich erhöht. Der klinische Nachweis muss sehr solide sein. Das beginnt bei der klinischen Bewertung, die oft durch klinische Prüfungen vor der Inverkehrbringung unterstützt werden muss. Labquality kann hier als Ihr vertrauenswürdiger CRO agieren.
Regulatorischer Lebenszyklus
Nach der CE-Kennzeichnung, der FDA-Freigabe oder -Zulassung oder einer anderen nationalen Vertriebszulassung muss der Hersteller die technische Dokumentation fortschreiben und die Behörden ggf. über Änderungen informieren. Labquality beschäftigt Expert*innen zur Überwachung der regulatorischen Landschaft. Sie veranlassen bei Bedarf die erforderlichen Aktivitäten, um die Medizinprodukte auf den gewünschten Märkten zu halten. Die meisten Märkte erfordern eine aktive Überwachung nach dem Inverkehrbringen (je nach Risikostufe) und eine aktive Berichterstattung an die Behörden. Für diese Aufgabe bietet Labquality den Dienst Post Market Surveillance as a Service (PMSaaS) an. Ein Produkt auf mehreren Märkten gleichzeitig zu halten, erfordert einen gewissen Aufwand und eine strukturierte Vorgehensweise.
.jpg)
Labquality
Wie können wir Sie unterstützen?
Labquality kann Sie bei folgenden Aktivitäten unterstützen:
Planung der regulatorischen Pfade
Dokumentierung der Zielmarktanforderungen in Zulassungsplänen
Qualifizierung und Klassifikation für alle Zielmärkte
Unterstützung bei Auslegungs- und Entwicklungsprozessen
Unterstützung bei allen Unterlagen für die technische Dokumentation
Klinische Bewertung: Planung und Berichterstattung
Klinische Prüfungen: Planung, Datenmanagement, Umsetzung und Berichterstattung
